تفاوت نیتروژن و اکسیژن در چیست؟
سپهر گاز کاویان، دارنده گواهینامه ISO17025، تأمین کننده نیتروژن (ازت) ، اکسیژن و سایر گازها و مایعات صنعتی و آزمایشگاهی با خلوص بالا و قیمت مناسب- تماس با شماره های 02146837950 و 02146835980-09033158778

نیتروژن و اکسیژن هر دو در یک بخش از جدول تناوبی ظاهر می شوند و باعث می شود فاز گاز را ترجیح دهند. آنها در دمای بسیار پایین ( مشابه دمای نیمه تاریک ماه) مایع می شوند و در نقطه جوش بسیار نزدیک به هم، به گاز تبدیل می شوند.
ویژگی های نیتروژن و اکسیژن
نیتروژن گازی بی بو، بی رنگ و بی مزه است. این عنصر فراوان ترین عنصر در اتمسفر است و مولکول دو تمی آن، 78 درصد از هوایی که تنفس می کنیم را تشکیل می دهد.
اکسیژن نیز گازی بی بو، بی رنگ و بی مزه است، اما فراوانی آن در جو بسیار کمتر است و تنها 21 درصد از هوایی که تنفس می کنیم را تشکیل می دهد.
Nitrogen یک گاز غیر واکنشی و بی اثر است، در حالی که اکسیژن بسیار واکنش پذیر است و با بسیاری از عناصر دیگر ترکیباتی را تشکیل می دهد.
ویژگی های فیزیکی مشترک نیتروژن و اکسیژن
نیتروژن و اکسیژن دارای خواص فیزیکی مشابه زیادی هستند. قرار داشتن هر دو در سمت راست دوره دوم جدول تناوبی باعث ایجاد مولکول های دو اتمی کوچک می شود که به شدت فاز گاز را ترجیح می دهند.
گازهای نیتروژن و اکسیژن در نقطه جوش بسیار کم، به گاز تبدیل می شوند که به طرز شگفت انگیزی نزدیک به هم هستند، و فقط در دمای نزدیک به دمای نیمه تاریک ماه مایع می شوند.
مقایسه ساختار و واکنش پذیری نیتروژن و اکسیژن
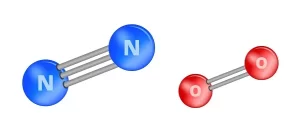
ویژگی های اکسیژن
O متعلق به گروه 16 جدول، اتم های آن دو الکترون کمتر از اوکتت هستند. یعنی دو اتم O با تشکیل یک پیوند دوگانه به هم متصل شده و دو جفت الکترون – به عبارت دیگر، در مجموع چهار الکترون- برای رسیدن به اکتت به اشتراک می گذارند.
ویژگی های نیتروژن
N در گروه 15 جدول تناوبی قرار دارد، و اتم های آن سه الکترون کمتر از اکتت دارند. بنابراین انتظار می رود N2 حاوی شش الکترون ( سه جفت) مشترک باشد که در برای تشکیل یک پیوند سه گانه به هم متصل می شوند.
مقایسه ساختار نیتروژن و اکسیژن
پیوند سه گانه N2 بسیار پایدارتر از پیوند دوگانه O2 است و به طور متوسط به 941 کیلوژول انرژی نیاز دارد تا یک مول از نیتروژن دو اتمی را به اتم جدا کند.
این پایداری شدید N2 باعث میشود که بر خلاف اکسیژن، نیتروژن نتواند در بسیاری از انواع واکنشهای شیمیایی– واکنشهایی مانند احتراق و تنفس که به تأمین انرژی خانهها، وسایل نقلیه و حتی خودمان کمک میکند– شرکت کند
گازهایی که در دماهای بسیار پایین مایع می شوند را کرایوژن می نامند و ازت مایع یکی از پرمصرف ترین کرایوژن های امروزی در جهان است.
بیشتر بخوانید | کاربرد نیتروژن | N2 | ازت مایع برای پوست
روش های تهیه
تهیه N2
- غشاها برای مقادیر و خلوص کمتر مناسب هستند. هر چه دما بیشتر باشد، راندمان تولید N2 بالاتر است.
- با جذب نوسان فشار (PSA) می توان به خلوص بالا (97 تا 99999 درصد نیتروژن) و ظرفیت تولید نسبتاً بالا دست یافت. می توان به خلوص بالاتری هم رسید، اما مصرف هوای فشرده بیشتر است.
- گازهای خالص را می توان با سرد کردن هوا تا زمانی که به مایع تبدیل شود از آن جدا کرد. سپس اجزا بر اساس دماهای مختلف جوش جدا می شوند.
این روش گازهایی با خلوص بالا و ظرفیت بالا تولید می کند اما نیاز به صرف هزینه و انرژی بیشتری دارد.
مازاد گازهای تولید شده به صورت ازت مایع توزیع می شود یا این ازت مایع در سیلندرهای فشار قوی تبخیر و فشرده می شود.
تهیه O2
در مقایسه با Nitrogen، غشایی برای تولید مستقیم Oxygen در بازار وجود ندارد، بنابراین راه های ممکن تولید فقط روشهای PSA و تقطیر جزءبه جزء است.
- در کنار PSA می توان VPSA را نیز استفاده کرد. V نشان دهنده خلاء است. تفاوت این روش با PSA تنها مربوط به تفاوت فشار است (PSA از 6 تا 10 بار، VPSA حدود 0.5 بار). VPSA معمولا برای ظرفیت های بالا استفاده می شود.
با PSA و VPSA می توان به حداکثر خلوص 95٪ رسید. گازهای دیگر کم و بیش گازهای نجیب مانند هلیم، آرگون و غیره هستند.
- با روش تقطیر جزءبه جزء می توان به خلوص بالاتری رسید، زیرا جداسازی بر اساس نقاط جوش متفاوت گازها انجام می شود. همانند نیتروژن، اکسیژن تولید شده تقطیر جزء به جزء به صورت اکسیژن مایع یا فشرده به مشتریان نهایی توزیع می شود.
دلیل مقدار متعادل واکنش در جو
واکنش پذیری O2 می تواند یک شمشیر دولبه باشد. مهندسان ناسا این را با وحشت طی یک آزمایش تمرین زمینی با خدمه آپولو 1 آموختند.
برای تسهیل تنفس و همچنین کاهش فشار بیرونی بدنه در خلاء فضا، کابین فرماندهی آنها با اکسیژن خالص پر شد. متأسفانه یک ولتاژ لحظه ای در یکی از اجزای کابین وجود داشت و همین برای ایجاد آتش سوزی کافی بود. هر سه فضانورد در عرض چند ثانیه جان خود را از دست دادند.
این فاجعه اهمیت همکاری نیتروژن و اکسیژن در جو ما را نشان می دهد. بعداً مأموریت های آپولو با استفاده از مخلوطی از نیتروژن و اکسیژن برای کاهش خطر آتش سوزی راه اندازی شدند.
اهمیت حضور نیتروژن و اکسیژن در کنار یکدیگر
خوشبختانه نیتروژن و اکسیژن دارای واکنشپذیری متفاوتی هستند.
نیتروژن و اکسیژن بطور هماهنگ عمل میکنند تا مقدار متعادلی از واکنشپذیری را در اتمسفر ما ارائه دهند، به هوا اجازه میدهند تا زندگی را امکان پذیر کند، بدون اینکه یک رعد و برق و آتشسوزی خود به خودی کل سیاره ما را از بین ببرد!
تفاوت در کاربردهای نیتروژن و اکسیژن
Oxygen برای فرآیندهای متابولیک اکثر موجودات زنده ضروری است. همچنین باعث تسریع سوختن می شود که برای صنعت فولاد و شیشه مفید است.
O2 بسیار واکنش پذیر است و تقریباً با همه عناصر به جز عناصر بی اثر واکنش می دهد.
به همین دلیل است که از آن در انواع کاربردهای که از واکنش پذیری O2 بهره می برند، در زمینه هایی از قبیل پزشکی، دارویی، آبزی پروری، گاز خوراک برای ژنراتورهای ازن، دمیدن شیشه، کاهش NOx برای مشعل های سوخت، شستشوی اکسیژن، جوشکاری و … استفاده می شود.
بیشتر بخوانید | کاربردهای اکسیژن
کاربردهای N2 متکی بر بی اثر بودن آن است و اهمیت کاربرد آن در ایجاد یک جو بی اثر و غیرواکنشی است.
بین اتم های N پیوند بسیار قوی وجود دارد که N2 را بسیار پایدار می کند بنابراین نیازی به شرکت در واکنش های شیمیایی ندارد. با توجه به این خواص، Nitrogen در صنایع غذایی، فرآوری فولاد، الکترونیک و کاربردهای مشابه استفاده می شود.
بیشتر بخوانید | کاربردهای نیتروژن | تولید دی اکسید نیتروژن
مقایسه ویژگی های نیتروژن و اکسیژن | |
|
نیتروژن |
اکسیژن |
| عنصری شیمیایی متعلق به گروه 15 جدول تناوبی. | عنصری شیمیایی متعلق به گروه 16 جدول تناوبی. |
| عدد اتمی آن 7 است. | عدد اتمی آن 8 است. |
| نماد شیمیایی آن N است. | نماد شیمیایی آن O است. |
| فرمول شیمیایی گاز نیتروژن N2 است. | فرمول شیمیایی گاز اکسیژن O2 است. |
| گازی که در هوا به مقدار حداکثر یعنی حدود 78% وجود دارد. | گازی ضروری که در هوا به مقدار کم و حدود 21%وجود دارد. |
| در بدن حیوانات نیز وجود دارد اما به مقدار کم. | برای زنده ماندن توسط موجودات زنده استنشاق می شود. |
| در بسیاری از صنایع مانند کروماتوگرافی گازی در داروسازی استفاده می شود. | در بیمارستان ها، برای جوشکاری مواد و سایر صنایع استفاده می شود. |
| برای پر کردن تایر خودروها، بسته بندی مواد غذایی و … استفاده می شود. | O2 خالص برای پمپاژ آب کثیف برای تمیز کردن آب استفاده می شود.
در ارتفاعات بالا سطح Oxygen کم است، بنابراین ورزشکاران برای صعود به ارتفاعات از سیلندر O2 استفاده می کنند. |




